科技日報記者 趙漢斌
記者8日從中國科學院昆明動物研究所獲悉,該所研究員姚永剛、張登峰帶領團隊,攜手解析了阿爾茨海默病小鼠脈絡叢在發病早期的細胞和分子病理變化特征,為其發病機制研究提供了新視角,并有望推動早期干預策略的研發。相關研究成果近期發表在國際學術期刊《分子神經退行性疾病》上。
人的大腦時刻處于腦脊液的保護之中。脈絡叢是腦脊液的分泌組織,也是血液—腦脊液屏障,在神經系統中扮演著重要角色。在神經退行性疾病如阿爾茨海默病、帕金森病等患者中,脈絡叢體積會顯著增大,且年輕健康小鼠腦脊液移植能改善老年或阿爾茨海默病模型小鼠認知功能,這凸顯了脈絡叢在腦疾病中的關鍵作用。
研究團隊新構建了阿爾茨海默病模型的脈絡叢單細胞轉錄圖譜,囊括了迄今為止最大數量的脈絡叢單細胞。通過轉錄組分析、原位驗證及體外靶點干預實驗,他們全面闡釋了病理早期脈絡叢的細胞和分子病理變化特征。
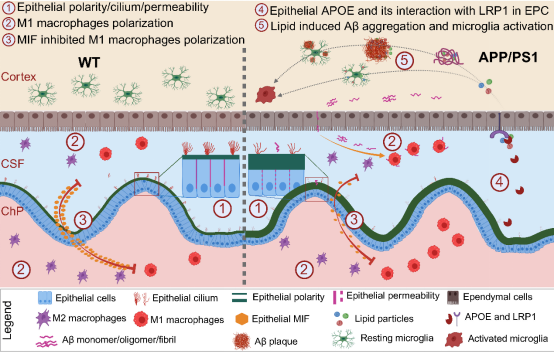
研究發現,脈絡叢由上皮細胞、免疫細胞、內皮細胞等6大類細胞組成,其中上皮細胞約占細胞總數的四分之三,其通過緊密連接形成屏障結構,還高表達多種阿爾茨海默病重要基因。相比于同性別的正常對照小鼠,雄性模型小鼠脈絡叢中上皮細胞比例明顯降低,線粒體能量代謝下降,纖毛組分減少且極性改變,上皮細胞通透性增加,屏障功能受損。此外,脈絡叢還包含多種免疫細胞亞群,部分細胞亞群表達增殖信號,呈現出“淋巴結樣”免疫細胞原位增殖的特性。
在早期患病的小鼠中,脈絡叢上皮細胞的巨噬細胞遷移抑制因子表達下調,引發免疫細胞通信紊亂,導致巨噬細胞激活。脈絡叢中的巨噬細胞能夠穿越脈絡叢進入腦脊液,與室管膜細胞直接作用,并通過增加配體分泌,增強與室管膜受體的互作,進而促進皮層組織脂質積累和小膠質細胞激活等下游病理效應。
此項研究還發現脈絡叢的基因表達譜存在明顯的性別差異,為后續基于性別差異的病理機制研究提供了數據支持,也為通過靶向脈絡叢以干預腦實質病變的早期干預策略研發奠定了科學基礎。